过去,主动脉弓疾病的治疗非常棘手。很多患者需要开胸大手术,有时还要让心脏暂时停下来,借助体外循环完成修复。对于身体条件好的患者来说,这已经是高难度手术;而对于高龄、心肺功能差、曾经做过主动脉手术的患者来说,风险更是巨大。这些人不是不想手术,而是根本无法做开胸手术。最近,美国食品药品监督管理局(FDA)批准了一款名为Nexus的新型主动脉弓支架上市[1],它针对的人群,正是这部分过去不能开刀的高危患者。
对于已经接受过多种治疗的晚期乳腺癌患者,尤其是那些对内分泌治疗和CDK4/6抑制剂(一类广泛使用的靶向药)产生耐药的患者,治疗选择往往非常有限。近日,美国食品药品监督管理局(FDA)授予了一款在研新药TER-2013快速通道资格,为这一困境中的患者群体带来了新的希望。
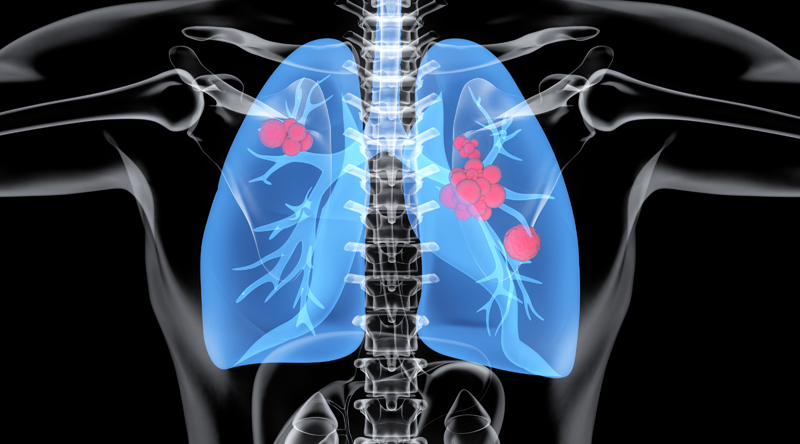
美国食品药品监督管理局(FDA)近日授予在研新药VS-7375快速通道资格,用于治疗携带KRAS G12D突变的晚期或转移性非小细胞肺癌(NSCLC)患者。这些患者此前已接受过铂类化疗和PD-(L)1免疫检查点抑制剂治疗。
近日,法国Enterome公司宣布,美国食品药品监督管理局(FDA)已授予其开发的新型癌症疫苗EO2463孤儿药资格(ODD),用于治疗低肿瘤负荷、处于观察等待阶段的惰性非霍奇金淋巴瘤(iNHL)患者。EO2463是一种现成可用的多靶点癌症疫苗,旨在调动患者自身免疫系统,攻击惰性非霍奇金淋巴瘤中的恶性B细胞。
根据2026年美国临床肿瘤学会(ASCO)年会公布的3期CROWN临床试验7年随访数据,洛拉替尼(Lorbrena)相比克唑替尼(Xalkori),在晚期ALK阳性非小细胞肺癌患者中显示出更持久的长期疗效优势,包括对脑转移患者也有明显获益。
近日,英国Greywolf Therapeutics公司公布了EMITT-1研究6个已完成1b期扩展队列的数据。分别是:非小细胞肺癌(NSCLC)、尿路上皮癌(UC)、肝细胞癌(HCC)、微卫星稳定型结直肠癌(无肝转移)、头颈部鳞状细胞癌(SCCHN)及宫颈癌队列。该研究正在评估新药GRWD5769联合PD-1抑制剂Cemiplimab,治疗既往接受PD-1抑制剂后产生继发耐药的患者,以及无肝转移的微卫星稳定型结直肠癌患者的效果。
一项名为HER2CLIMB-05的III期临床试验,在2026年美国临床肿瘤学会(ASCO)年会上更新了其详细数据,结果显示,在标准一线维持治疗中加入图卡替尼(Tucatinib),能够为HER2阳性(HER2+)转移性乳腺癌患者带来显著的生存获益。这项国际多中心研究证实,无论患者的激素受体(HR)状态、是否存在脑转移,也无论她们是初次诊断即为晚期(称为de novo)还是复发后进入晚期,都能从这一新方案中获益。
根据在2026年美国临床肿瘤学会(ASCO)年会上公布的1/1b期StrateGIST-1研究的数据,新药Velzatinib在晚期或转移性胃肠道间质瘤(GIST)患者中,无论KIT突变状态如何、无论处于哪一治疗阶段,均展现出强劲且持久的临床活性。同时,研究人员通过抽血检测发现,治疗前就能检测到KIT9号外显子突变的患者,使用Velzatinib后的效果尤其明显。Velzatinib(研发代号IDRX-42)所属公司为英国葛兰素史克(GSK)公司,目前仍处于临床研究阶段,尚未获批上市。
根据2026年美国临床肿瘤学会(ASCO)年会上公布的一项2a期研究结果,新药Atebimetinib联合改良版的吉西他滨和白蛋白紫杉醇方案(简称mGnP),治疗一线转移性胰腺导管腺癌(PDAC)患者时,展现出良好的耐受性以及令人鼓舞的总生存获益。
脑转移是几乎所有癌症患者恐惧的梦魇。人类的大脑很脆弱,也很重要,它管着我们说话、走路、记忆甚至性格,也涉及了一个人基本的生活自理能力和尊严。一旦肿瘤转移到大脑,则患者会迅速陷入巨大危机:不治疗危及生命,治疗的话又有诸多限制——比如手术、放疗等局部治疗手段稍有不慎,可能直接影响到关键身体功能,让人丧失基础的行动、语言、思维能力;比如很多抗癌药被血脑屏障阻碍,无法入脑。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业








 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估