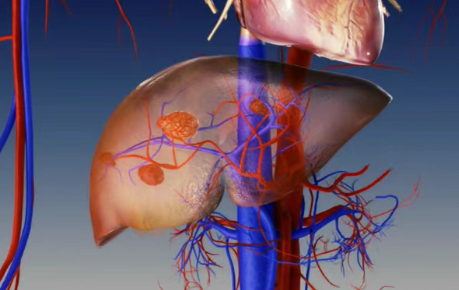
肝细胞癌(HCC)一直是临床治疗中的难点之一。多数患者在确诊时已失去手术机会,只能依赖局部或全身治疗来控制病情。长期以来,经肝动脉化疗栓塞(TACE)被视为这一阶段的主要治疗手段,但疗效始终存在瓶颈。2025年7月,SIR-Spheres Y-90树脂微球(中文称作钇-90)获得美国食品药品监督管理局(FDA)批准,用于治疗不可切除的肝细胞癌(HCC)。
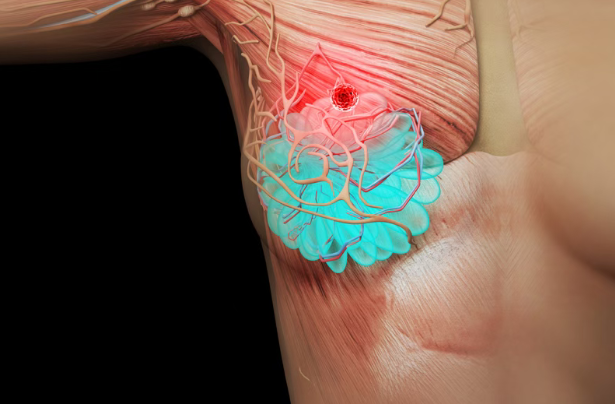
近日,美国Celcuity公司公布了其开发的新药Gedatolisib,在3期VIKTORIA-1临床试验中PIK3CA野生型患者队列的疗效和安全性结果。该队列包括激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)、PIK3CA野生型的晚期乳腺癌患者,这些患者在接受CDK4/6抑制剂和芳香化酶抑制剂治疗期间或之后出现疾病进展。研究结果显示,在PIK3CA野生型晚期乳腺癌中,Gedatolisib联合Fulvestrant(以及联合Palbociclib),可显著改善无进展生存期,意味着有效帮助患者控制了疾病进展。研究结果发表于医学学术期刊《临床肿瘤学杂志》上。
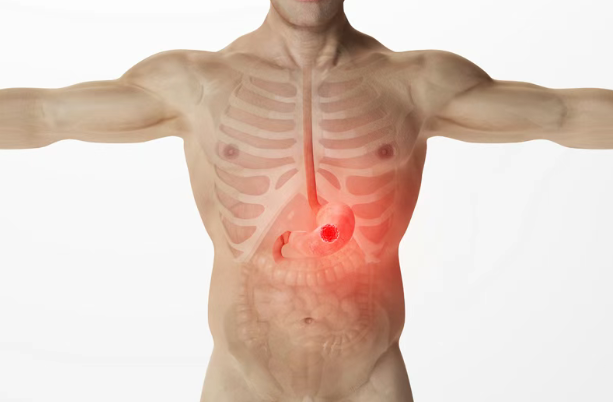
近日,美国NovaBridge Biosciences公司宣布,已就新药Givastomig在一线HER2阴性、CLDN18.2阳性、PD-L1阳性胃癌/胃食管交界癌患者中的加速批准潜力,与美国食品药品监督管理局(FDA)达成一致意见。这一进展基于近期公布的1b期临床试验(临床试验注册号:NCT04900818)剂量扩展数据基础上。这是Givastomig首次用于人体研究,主要评估其在晚期实体瘤中的安全性、耐受性、药代动力学、药效学以及初步抗肿瘤活性,包括单药和联合治疗方案。研究结果显示,Givastomig疗效显著且耐受性良好。
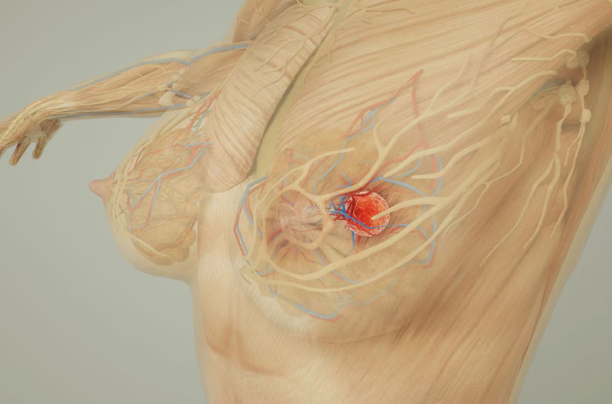
对于乳腺癌脑膜转移患者来说,以往几乎没有有效的治疗选择。如今,来自美国MD安德森癌症中心的研究人员发现,由靶向药治疗组合(Tucatinib和Trastuzumab)联合化疗药Capecitabine组成的方案,能帮助部分乳腺癌脑膜转移患者缓解症状并延长生存。这项发表于权威学术期刊《Nature Cancer》的2期研究,共纳入17名新诊断为脑膜转移且HER2阳性的女性乳腺癌患者。
近日,一项发表在权威期刊《Nature》的研究显示,美国加州大学旧金山分校(UCSF)的科学家,首次实现了体内制造CAR-T细胞,不再需要把细胞取出体外改造。动物实验显示,新疗法1次注射后2周内几乎清除了全部癌细胞,且对多发性骨髓瘤、白血病甚至实体瘤都有效。如果未来在人身上验证成功,有望大幅降低费用、缩短等待时间,让更多患者用得上CAR-T疗法!
近日,美国CytomX Therapeutics公司宣布,其开发的新型抗体偶联药物(ADC)Varsetatug Masetecan(研发代号Varseta-M),在后线转移性结直肠癌(即经过多轮治疗仍进展的患者)的1期临床试验中,展现出令人鼓舞的疗效和良好的安全性。正在进行的1期研究名为CTMX-2051-101,数据截止时间为2026年1月16日。
近日,美国食品药品监督管理局(FDA)批准Teclistamab(商品名Tecvayli)联合Daratumumab透明质酸酶-fihj(该联合方案简称Tec-Dara),用于治疗既往至少接受过一线治疗(包括蛋白酶体抑制剂和免疫调节剂)的成人复发或难治性多发性骨髓瘤患者。
过去,罹患晚期肝癌往往意味着患者生存时间非常有限,能活过5年的人非常少;而现在,IMJUDO双免疫方案让大约每5个患者中就有1个人能够活过5年,这在几年前几乎是无法想象的!
近日,3期FLAMINGO-01临床试验的新研究数据公布[1],一种名为GLSI-100的乳腺癌疫苗,将乳腺癌术后高复发风险患者的年复发率降到了不到1%,效果明显优于当前标准治疗。
近日,美国Citius Oncology公司公布了一项1期临床试验的积极结果:前沿药Lymphir联合PD-1抑制剂帕博利珠单抗(Keytruda),在复发或难治性妇科肿瘤患者(包括卵巢癌和子宫内膜癌)中显示出初步临床活性,并且安全性可控。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业







 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估