近日,3期AFFIRM-205临床研究公布的新结果显示,已经对激素治疗(内分泌治疗)耐药的晚期乳腺癌患者,在原本的标准治疗基础上,加用名为afuresertib的新药,可以大幅延长肿瘤控制时间,同时显著降低患者死亡风险。
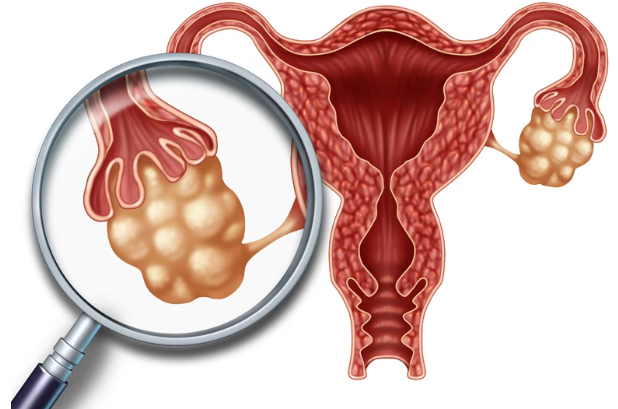
近日,2期PYNNACLE(NCT04585750)临床研究在2026年妇科肿瘤学会(SGO)年会上公布了中期结果。数据显示,TP53口服靶向药Rezatapopt(PC14586)在多重耐药的难治性卵巢癌患者中,让44.4%的人肿瘤大幅缩小或消失。该药起效速度很快(中位1.3个月),且疗效持久性良好。
2026年4月15日,国际权威期刊《新英格兰医学杂志》发表了前沿药物Zongertinib(商品名:HERNEXEOS)的新研究结果。在1b期Beamion LUNG-1研究(临床试验注册号:NCT04886804)中,Zongertinib在未接受过治疗、携带HER2突变的晚期非小细胞肺癌(NSCLC)患者中,展现出显著且持久的抗肿瘤疗效,同时整体安全性可控。
美国食品药品监督管理局(FDA)已授予Eftilagimod alfa(又名IMP321,简称Efti)孤儿药资格,用于治疗软组织肉瘤(STS)。FDA的孤儿药计划,用于鼓励针对罕见疾病(在美国患者少于20万人)的药物研发,提供多项激励措施。
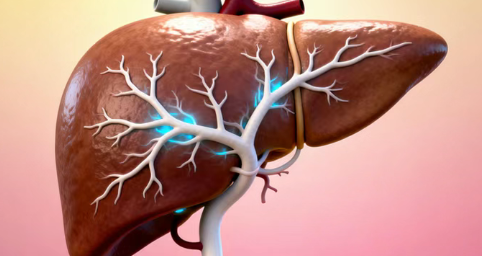
时至今日,大部分患者仍然只能靠化疗控制肿瘤,药物选择很有限。不过近期好消息传来,胆管癌终于将要迎来一款精准靶向药——zenocutuzumab。目前,该药的开发商已经向美国食品药品监督管理局(FDA)提交了上市申请。同时,该药也被写进了权威的NCCN癌症诊疗指南(肿瘤医生的指导手册)。
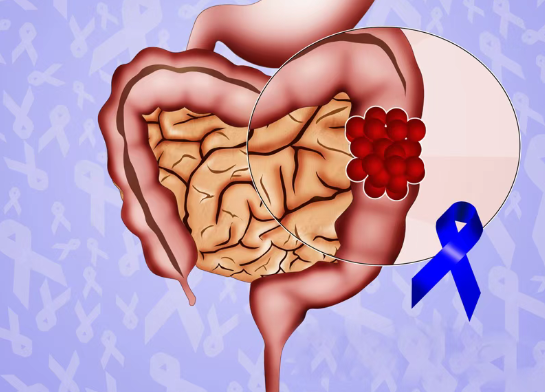
新型免疫治疗药物PDS01ADC在转移性结直肠癌(mCRC)患者中显示出早期疗效,尤其是在既往治疗后疾病进展且伴有肝转移的患者中。由美国国家癌症研究所(NCI)主导的2期临床试验的中期结果显示,该疗法具有较高的应答率和令人鼓舞的生存结局,提示其可能有助于填补这一患者群体长期未被满足的治疗需求。当PDS01ADC与肝动脉灌注泵(HAIP)化疗联合使用时,似乎可以增强免疫系统识别并攻击癌细胞的能力。尽管这些结果基于较小规模患者,但仍凸显了将靶向免疫治疗与区域化疗结合,有望改善治疗效果的潜力。
在今天,越来越多肺癌患者查出EGFR突变,会遇到一个特别现实的问题:一线治疗(第一次治疗)到底该选哪个方案?癌症一线治疗通常会给患者使用经临床研究证实疗效特别好、有效率特别高的方案。后面如果方案耐药了,再换的其他方案就叫二线治疗,再然后就是三线方案,以此类推。之所以会有这个疑问,主要在于目前针对EGFR突变肺癌的获批方案中,有3个疗效非常不错,都可能适合一线治疗
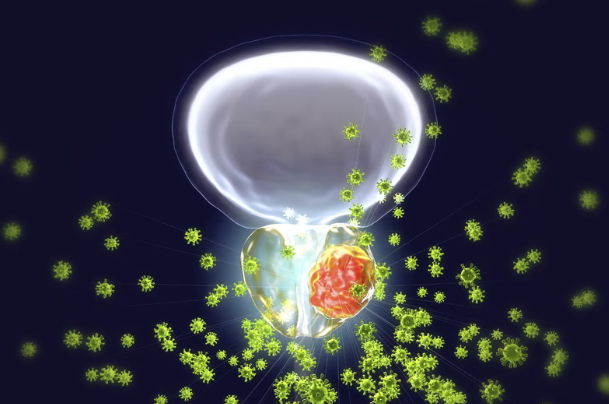
近日,美国Vir Biotechnology公司宣布,在评估新药VIR-5500的1期试验中,3个扩展队列中的其中1个队列已完成首位患者给药。目前,VIR-5500正在一项1期临床试验中(临床试验注册号:NCT05997615)接受评估。该研究既评估VIR-5500单药在多线治疗后的转移性去势抵抗性前列腺癌(mCRPC)中的安全性和疗效,也在联合用药中探索其在早线(治疗刚开始用的阶段)mCRPC及转移性激素敏感性前列腺癌(mHSPC)中的效果。
根据2026年妇科肿瘤学会(SGO)年会(女性癌症会议)上公布的2期RAMP201试验(临床试验注册号:NCT04625270)的更新数据,Avutometinib联合Defactinib,在低级别浆液性卵巢癌(LGSOC)患者中显示出持久疗效,且未出现新的安全性信号。
近日,在2026年的妇科肿瘤学会年会(SGO)上,1/2期ENGOT-cx8/GOG-3024/innova TV 205研究显示,在复发或转移性宫颈癌的一线(初始)治疗中,一种四联组合让65.8%的患者肿瘤明显缩小,其中18.4%的人肿瘤全消失!
 红杉资本(中国)被投企业
红杉资本(中国)被投企业






 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估