近日,在2026年的妇科肿瘤学会年会(SGO)上,一项2期临床研究显示,已对含铂双药化疗方案出现耐药进展的复发或转移性宫颈癌(含鳞癌、腺癌或腺鳞癌)患者,可使用前沿的抗体偶联药物Sac-TMT联合免疫疗法。数据显示,90%的此类患者病情得到控制,其中51%的患者肿瘤明显缩小或消失!
2026年4月13日,美国Revolution Medicines公司公布了3期RASolute302临床试验的积极结果。该试验评估了Daraxonrasib(RMC-6236)在既往接受过治疗的转移性胰腺导管腺癌(PDAC)患者中的疗效。研究结果显示,与标准化疗相比,每日口服一次Daraxonrasib,在无进展生存期(PFS)和总生存期(OS)方面均带来了具有统计学意义且临床意义明确的改善。
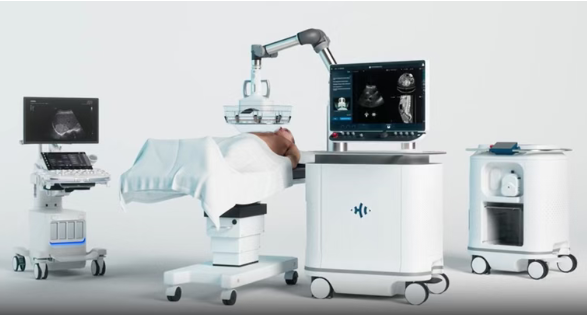
不用开刀、不用打针、不用放疗,真的可以治疗肝肿瘤吗?近日,美国哈肯萨克子午线泽西海岸大学医学中心(JSUMC)的Gregory Tiesi医生,在接受CURE®平台采访时,详细讲解了抗肿瘤新技术——Histotripsy(组织碎化术),包括它的工作原理、适用人群以及患者的实际治疗体验。简单来说,这项技术利用聚焦超声来打碎肝肿瘤,不需要手术或传统消融,为患者提供了一种全新的无创治疗选择。
近日,英国生物技术公司Trogenix Ltd宣布,其一项突破性研究成果已发表于国际权威期刊《Nature》。研究显示,在一种高度模拟人类胶质母细胞瘤的侵袭性脑癌模型中,仅通过一次治疗,就在83%的病例中实现肿瘤完全清除,并在长达11个月的随访中未出现复发,也未观察到明显毒性。这种疗法本质上是一种新型基因治疗:通过病毒将特制的基因开关送入癌细胞,在细胞内部同时实现直接杀死肿瘤+激活免疫系统的双重作用。
根据韩国Celltrion公司发布的新闻稿,美国食品药品监督管理局(FDA)已授予新药CT-P71快速通道资格,用于治疗局部晚期或转移性尿路上皮癌患者。FDA的快速通道制度,主要针对现有治疗手段效果不足的严重疾病,旨在让药物开发企业与美国食品药品监督管理局(FDA)在整个研发过程中更快速沟通,从而加快新药研发进程。
根据韩国生物技术公司ABL Bio发布的一份新闻稿,美国食品药品监督管理局(FDA)已授予Tovecimig(又名CTX-009)用于治疗胆道癌患者的孤儿药资格认定。2024年4月,Tovecimig已获得FDA授予的快速通道资格,用于转移性或局部晚期胆道癌患者的二线治疗。
美国生物技术公司Incyclix Bio正在开发一款新药,名为INX-315。INX-315是一种口服小分子药物,是一种新型、强效且具有高度选择性的CDK2抑制剂,用于治疗晚期及耐药性癌症,目前重点研究乳腺癌和卵巢癌。近日,INX-315又获得了500万美元的融资,用于推进INX-315在复发性晚期或转移性癌症患者中的1/2期临床试验。
近日,美国生物制药公司Nuvalent正式向美国食品药品监督管理局(FDA)提交了新型靶向药Neladalkib(NVL-655)的上市申请,用于治疗既往接受过ALK靶向治疗的晚期ALK阳性非小细胞肺癌(NSCLC)患者。
近日,加拿大生物技术公司Zymeworks宣布,美国食品药品监督管理局(FDA)已授予其开发的抗体偶联药物(ADC)ZW191快速通道资格,用于治疗晚期或转移性铂耐药卵巢癌(PROC)患者。FDA的快速通道资格,旨在加速对严重疾病有潜在治疗价值的药物研发和审批,使患者能更快获得急需的新疗法。
3期EMERALD-3试验的初步结果显示:对于无法手术但适合进行栓塞治疗的肝细胞癌(HCC)患者,PD-L1抑制剂Imfinzi(又名Durvalumab)联合CTLA-4抑制剂Imjudo(又名Tremelimumab)、靶向药仑伐替尼(Lenvatinib)以及经动脉化疗栓塞(TACE),相比单独使用TACE,显著改善了无进展生存期(PFS),意味着有效帮助患者控制了疾病进展。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业






 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估