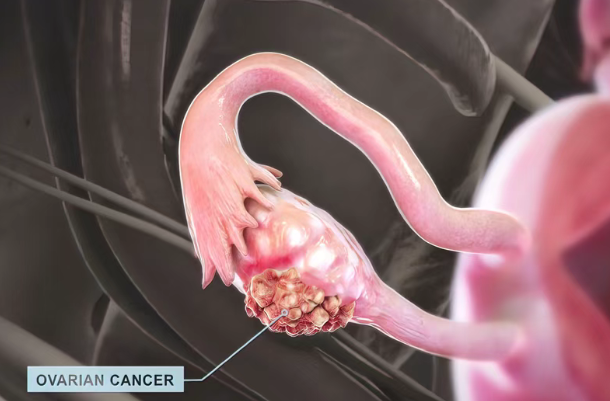
一项2期临床试验的结果表明,在基线CA-125水平升高的铂类耐药卵巢癌患者中,新药Elenagen联合化疗药吉西他滨(Gemacitabine),显著改善了总生存期。
近日,国际权威医学期刊《新英格兰医学杂志》发表了新药Rezatapopt的1期临床研究结果。该药针对携带TP53 Y220C突变、既往接受多线治疗且已发展为局部晚期或转移性实体瘤的患者,显示出初步抗肿瘤活性,整体安全性可控。在研究中,Rezatapopt在多种肿瘤类型中观察到客观缓解,包括卵巢癌和乳腺癌等。在全部入组患者中,客观缓解率为20%,意味着有20%的患者肿瘤显著缩小或完全消失。在KRAS为野生型且接受每日剂量至少1150mg治疗的患者中,客观缓解率为30%,意味着有30%的患者肿瘤显著缩小或完全消失。
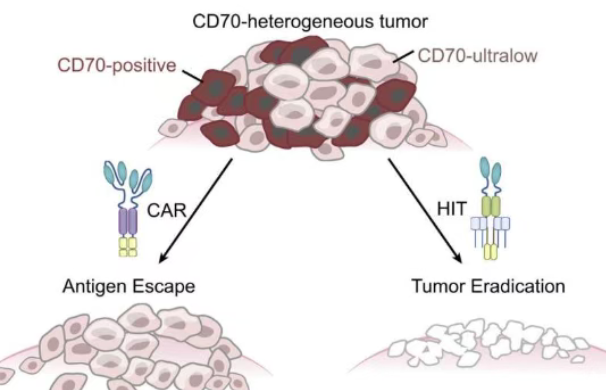
近日,美国哥伦比亚大学欧文医学中心的研究团队在权威期刊《Science》上发表了一项动物实验研究。他们把一种更灵敏的免疫细胞改造疗法用在了实体肿瘤上,结果发现:这种被称为HIT疗法的新一代细胞免疫疗法,能精准识别和有效灭杀实体瘤里藏得深的癌细胞,在小鼠的肾癌、胰腺癌和卵巢癌模型中,肿瘤被该疗法彻底清理掉,且没有误伤正常组织。
胰腺癌一直被认为是难攻克的肿瘤之一。如今,一项发表于知名期刊《Nature Communications》的研究带来新的探索方向。在一项1期临床试验中,研究人员测试了一种名为mKRAS-VAX的胰腺癌疫苗,并联合两种免疫治疗药物Ipilimumab和Nivolumab,用于已完成手术的胰腺导管腺癌患者。结果显示,在12名患者中,有11人(近92%)产生了明显的抗癌免疫反应,并且整体安全性良好。
实体瘤一直是CAR细胞治疗领域公认的硬骨头。尽管CAR-NK细胞在血液肿瘤中展现潜力,但在实体瘤中始终难以发挥理想效果。如今,一项发表于国际顶刊《Nature》的研究带来关键突破。研究人员通过大规模基因筛选发现,只需增强一种名为OR7A10的受体,就能显著提升CAR-NK细胞在实体瘤中的抗肿瘤能力。
2026年2月19日,美国食品药品监督管理局(FDA)批准了Acalabrutinib(商品名Calquence)片剂和胶囊,与Venetoclax(商品名Venclexta)联合使用,用于治疗患有慢性淋巴细胞白血病(CLL)或小淋巴细胞淋巴瘤(SLL)的成人患者。
近日,瑞士Pilatus Biosciences公司宣布,美国食品药品监督管理局(FDA)已授予其开发的新药PLT012快速通道资格。用于治疗肝细胞癌(HCC)。此外,Pilatus Biosciences公司也正在其他实体瘤适应症中开发PLT012。FDA的快速通道资格旨在促进针对严重疾病且存在未满足医疗需求的疗法开发,并加快审评进程。该资格可使研发公司与FDA进行更频繁的沟通,并有机会获得优先审评、加速批准等资格。
近日,美国食品药品监督管理局(FDA)授予了爱万妥单抗突破性疗法认定,用于治疗一类病情非常棘手的头颈鳞状细胞癌(简称头颈鳞癌)患者。这类患者此前已经接受过大量治疗(包括化疗、免疫疗法),但病情仍在进展,后续治疗选择极为有限。支持本次FDA资格认定的是1b/2期OrigAMI-4临床研究。数据显示,在可评估疗效的患者中,45%的人肿瘤大幅缩小或消失。
近日,美国食品药品监督管理局(FDA)已全面批准Encorafenib、Cetuximab和含氟尿嘧啶化疗的三联治疗组合,用于治疗携带BRAF V600E基因突变的转移性结直肠癌成人患者。支持这项批准的是3期BREAKWATER临床试验,试验数据显示,相较于传统方案,新三联方案让更多患者肿瘤大幅缩小或消失,且肿瘤控制时间和总生存期均显著延长。
近日,1/2期临床试验(NCT04186520)的研究数据在2026年的移植与细胞治疗会议上公布。研究显示,一种名为LV20.19 CAR-T的双靶点细胞免疫疗法,在复发或难治性慢性淋巴细胞白血病患者中取得了相当不错的疗效。平均随访25个月时,接受这种新疗法的患者中,78%的患者实现了完全缓解(CR)或接近完全缓解(CRi),还有11%的患者病情大幅缓解(PR)。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业




 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估