2026年2月2日,美国Exelixis公司宣布,美国食品药品监督管理局(FDA)已接受Zanzalintinib联合Atezolizumab的新药申请,用于治疗既往接受过氟嘧啶类、奥沙利铂和伊立替康方案化疗的成人转移性结直肠癌患者;对于RAS野生型患者,还包括既往接受过抗表皮生长因子受体(EGFR)治疗的人群。FDA给予该申请标准审评,并将处方药使用者付费法案的目标审评日期定为2026年12月3日,意味着FDA将在2026年12月3日前给出是否批准的明确结果。
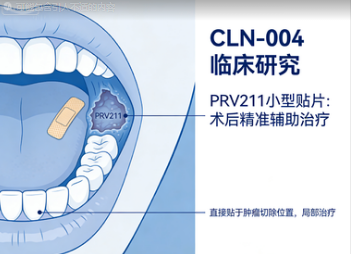
近日,在一项名为CLN-004的临床研究中,研究人员发现,一种看起来很像创可贴的小型贴片PRV211,可以在口腔癌患者手术结束后,直接贴在肿瘤被切除的位置,对局部进行精准的术后辅助治疗。
近日,美国Revolution Medicines公司宣布,其开发的新药RMC-5127,已正式进入人体临床研究阶段,并完成首位患者给药。这项首次人体试验RMC-5127-001(临床试验注册号:NCT07349537)为一项开放标签的1/1b期研究,纳入了携带RAS G12V突变的晚期实体瘤患者,包括胰腺导管腺癌(PDAC)、结直肠癌(CRC)和非小细胞肺癌(NSCLC)患者。这些患者在既往标准治疗(包括靶向治疗)后出现疾病进展或无法耐受相关治疗。
近日,美国生物制药公司Elevar Therapeutics宣布,已向美国食品药品监督管理局(FDA)提交了一项新药申请(NDA),寻求批准其研发药物lirafugratinib(RLY-4008)作为对携带FGFR2融合或重排的胆管癌患者的二线治疗方案。
近日,美国Novita Pharmaceuticals公司宣布,美国食品药品监督管理局(FDA)已授予其新药NP-G2-044孤儿药资格,用于治疗胰腺癌。FDA的孤儿药资格授予,旨在支持针对美国少于20万的罕见疾病患者的研究性疗法开发。胰腺癌是致命的恶性肿瘤之一,五年生存率约为12%,尤其在晚期疾病中有效治疗选择十分有限。
近日,美国生物制药公司Quetzal Therapeutics宣布,美国食品药品监督管理局(FDA)已授予QTX-2101快速通道资格,用于治疗急性早幼粒细胞白血病(APL)患者。FDA的快速通道资格,旨在促进严重疾病研究性疗法的开发并加快审评,凸显了急性早幼粒细胞白血病(APL)的严重性及在已有有效标准治疗下仍存在的未满足医疗需求。
来自加拿大伦敦健康科学中心研究院的研究人员近期发表了两项重要研究,显示一种被称为【粪便胶囊】的新技术,可能正在悄悄改变癌症治疗的效果和体验。研究成果发表在国际权威医学期刊《自然·医学》上。
根据近日发表在《新英格兰医学杂志》上的3期PATINA研究的数据,在激素受体阳性(HR+)、HER2阳性(HER2+)转移性乳腺癌的标准治疗基础上,加入CDK4/6抑制剂Palbociclib,可显著延长无进展生存期(延长超过15个月),意味着能有效帮助患者控制疾病进展。
根据发表于《Nature Medicine》的一项临床试验的数据,携带CDK通路或NF2基因改变的复发或进展性高级别脑膜瘤患者,在接受靶向药Verzenio(阿贝西利,abemaciclib)治疗后,显示出令人鼓舞的治疗反应。
近日,权威期刊《自然·医学》(Nature Medicine)发表了一项重磅研究成果:一种新型T细胞免疫治疗策略——自体多抗原靶向T细胞疗法,在胰腺癌患者的临床研究中显示出令人鼓舞的疗效。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业








 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估