美国上市新药
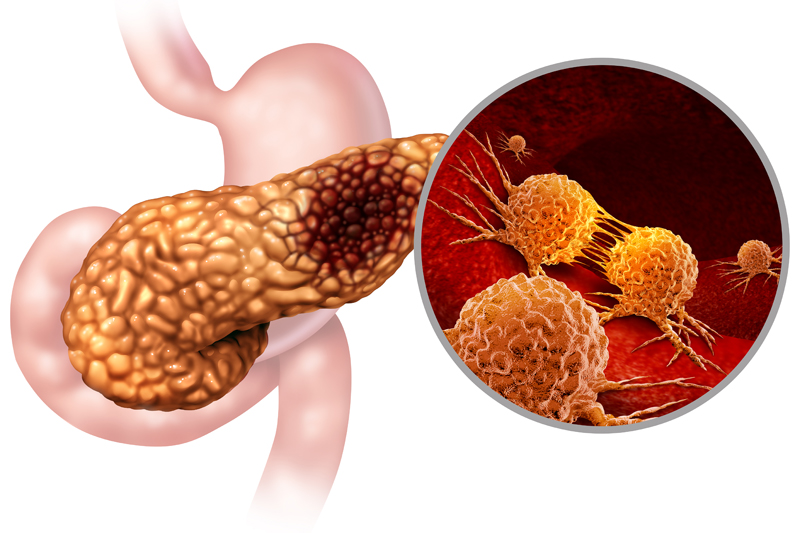
近日,美国Novita Pharmaceuticals公司宣布,美国食品药品监督管理局(FDA)已授予其新药NP-G2-044孤儿药资格,用于治疗胰腺癌。FDA的孤儿药资格授予,旨在支持针对美国少于20万的罕见疾病患者的研究性疗法开发。胰腺癌是致命的恶性肿瘤之一,五年生存率约为12%,尤其在晚期疾病中有效治疗选择十分有限。
近日,美国生物制药公司Quetzal Therapeutics宣布,美国食品药品监督管理局(FDA)已授予QTX-2101快速通道资格,用于治疗急性早幼粒细胞白血病(APL)患者。FDA的快速通道资格,旨在促进严重疾病研究性疗法的开发并加快审评,凸显了急性早幼粒细胞白血病(APL)的严重性及在已有有效标准治疗下仍存在的未满足医疗需求。
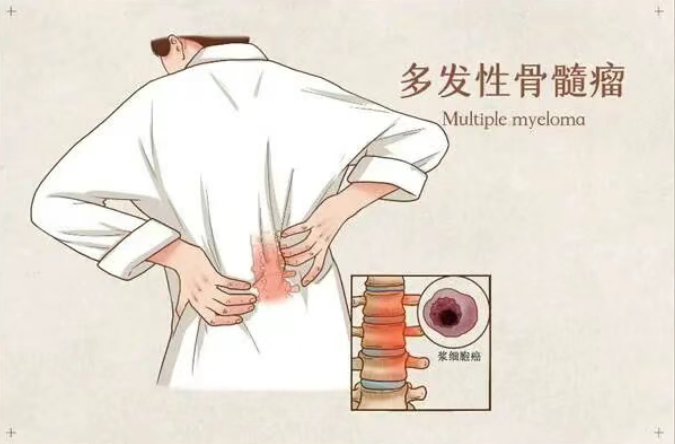
北京时间今天(1月28日)清晨,美国食品药品监督管理局(FDA)在官网更新:批准Darzalex Faspro + VRd方案,用于新诊断、且不适合自体造血干细胞移植的多发性骨髓瘤成人患者。
很多刚确诊的多发性骨髓瘤患者,会因为年龄或身体状况,不适合做干细胞移植。不能移植,则意味着他们剩下的有效治疗选择十分有限。近日,美国食品药品监督管理局(FDA)新批准上市的一款治疗方案,针对的正是此类患者。研究显示,这款由四种药物组成的四联方案疗效显著,超过一半的患者使用后实现了无癌状态!
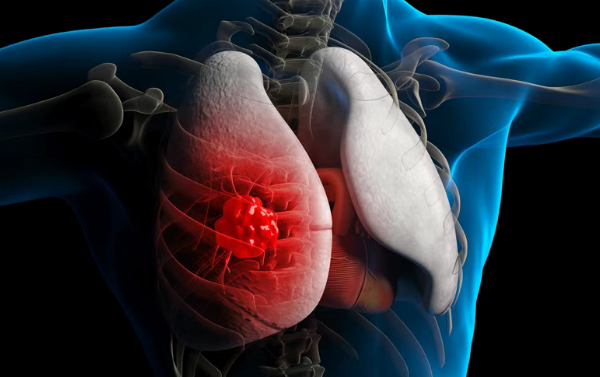
在肺纤维化这个大家族里,有两类患者,长期以来令医生和家属感到棘手。一类是特发性肺纤维化,另一类是进行性肺纤维化。这两类患者不同,但有一个共同点:疤痕会持续加重,肺功能会一步步往下走,而且很难刹住车。呼吸功能持续恶化,最终会危及患者生命。令人无奈的是,过去10多年来,肺纤维化几乎没有迎来真正意义上的新药突破。但现在,一款名为Nerandomilast(Jascayd)的新疗法已经出现。
美国食品药品监督管理局FDA已批准一种名为iSCIB1+的新型癌症疫苗治疗方案,用于晚期黑色素瘤患者的3期临床试验,这项试验计划于2026年启动。iSCIB1+是一种DNA质粒疫苗,它不是传统意义上的化疗药或免疫针,而是一段人工设计的DNA,进入人体后,化身免疫指挥官指导患者免疫系统,令其更精准、更持久地识别并攻击肿瘤细胞。
RMC-6236(通用名Daraxonrasib),是近几年国内患者高度关注的一款在研抗癌药物,尤其在胰腺癌患者群体中讨论热度极高。该药物可同时覆盖多种KRAS突变类型,在早期临床研究中显示出十分积极的疗效信号。对于长期缺乏有效靶向药选择的患者而言,这是一款被寄予厚望的潜力药物。
美国食品药品监督管理局(FDA)授予Gotistobart孤儿药资格,用于治疗鳞状非小细胞肺癌患者。Gotistobart是由德国BioNTec和美国OncoC4公司联合开发的一款抗癌药,是一款CTLA-4抑制剂类的免疫治疗药物。
美国食品药品监督管理局(FDA)已授予mRNA癌症疫苗BNT113快速通道资格,用于治疗人乳头瘤病毒16型阳性(HPV16阳性)且PD-L1表达阳性的头颈鳞状细胞癌(HNSCC)患者。这是一种与高危型人乳头瘤病毒感染相关的特定癌症类型。
美国食品药品监督管理局(FDA)已授予Soficabta geneGeleucel(简称Sofi-Cel)突破性治疗资格,用于治疗复发或难治性T细胞急性淋巴细胞白血病(T-ALL)和T细胞淋巴母细胞淋巴瘤(T-LBL)。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业


















 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估