美国上市新药
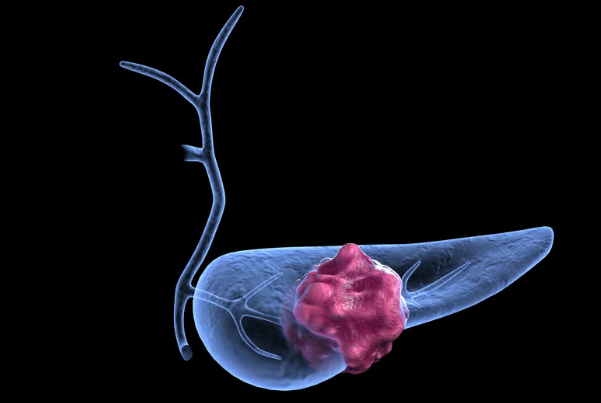
近日,美国Theriva Biologics公司宣布,已经和美国食品药品监督管理局(FDA)沟通确认,关于新药VCN-01(又名zabilugene almadenorepvec)用于转移性胰腺导管腺癌(PDAC)的3期临床研究设计。该研究计划将VCN-01与标准化疗联合使用。
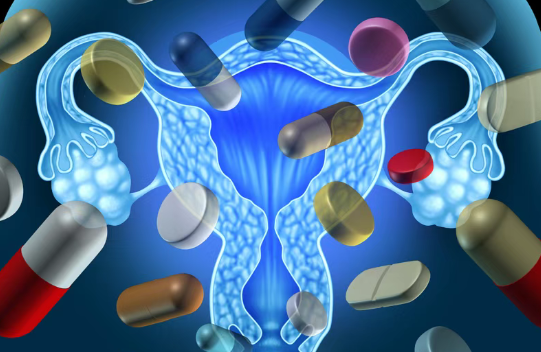
2026年3月25日,美国食品药品监督管理局(FDA)批准Relacorilant(商品名Lifyorli)与白蛋白紫杉醇(Abraxane)联合使用,用于治疗既往接受过1至3线全身治疗(之前的治疗中至少用过一次贝伐珠单抗)的成人铂耐药上皮性卵巢癌、输卵管癌或原发性腹膜癌患者。
3月20日,据百时美施贵宝新闻稿报道,美国食品药品监督管理局(FDA)批准纳武利尤单抗(nivolumab,商品名Opdivo)联合AVD化疗,用于成人及12岁以上、既往未治疗的Ⅲ/Ⅳ期经典型霍奇金淋巴瘤患者。对刚被确诊、正站在人生岔路口的患者和家属来说,这条消息的分量很直接:未来,晚期经典型霍奇金淋巴瘤的一线治疗,出现了一个更强、更有希望的新标准。
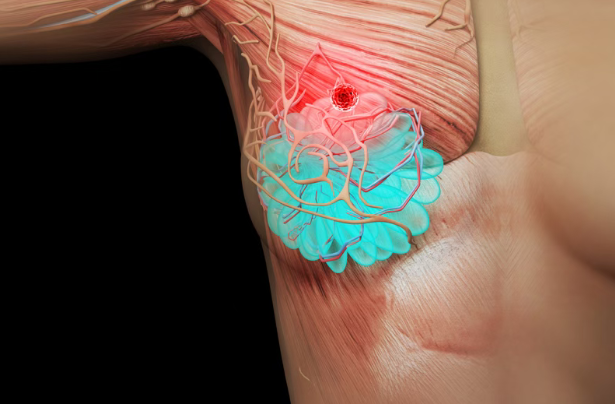
近日,美国Celcuity公司公布了其开发的新药Gedatolisib,在3期VIKTORIA-1临床试验中PIK3CA野生型患者队列的疗效和安全性结果。该队列包括激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)、PIK3CA野生型的晚期乳腺癌患者,这些患者在接受CDK4/6抑制剂和芳香化酶抑制剂治疗期间或之后出现疾病进展。研究结果显示,在PIK3CA野生型晚期乳腺癌中,Gedatolisib联合Fulvestrant(以及联合Palbociclib),可显著改善无进展生存期,意味着有效帮助患者控制了疾病进展。研究结果发表于医学学术期刊《临床肿瘤学杂志》上。
2026年3月20日,美国食品药品监督管理局(FDA)批准Nivolumab(商品名Opdivo)联合Doxorubicin、Vinblastine和Dacarbazine(AVD方案),用于12岁及以上、既往未接受治疗的III期或IV期经典型霍奇金淋巴瘤(cHL)患者。
近日,美国食品药品监督管理局(FDA)批准Teclistamab(商品名Tecvayli)联合Daratumumab透明质酸酶-fihj(该联合方案简称Tec-Dara),用于治疗既往至少接受过一线治疗(包括蛋白酶体抑制剂和免疫调节剂)的成人复发或难治性多发性骨髓瘤患者。
对于很多胃癌患者,尤其是晚期、HER2阴性的朋友来说,治疗选择一度非常有限。但这一状况正在不断改观。据3月16日NovaBridge发布的官方新闻,美国食品药品监督管理局(FDA)正式确认,胃癌创新双抗药物Givastomig符合加速审批路径。这意味着,这款新药有望缩短审批时间、更快来到患者身边。
美国Cullinan Therapeutics公司宣布,已完成向美国食品药品监督管理局(FDA)提交Zipalertinib的新药滚动申请(NDA),以获得加速批准,用于治疗此前接受过含铂化疗的局部晚期或转移性、携带EGFR外显子20插入突变的非小细胞肺癌患者。
对于许多HER2阳性乳腺癌病友来说,手术结束并不意味着抗癌之路的终点。尤其是那些在术前化疗(新辅助治疗)后,手术切除标本中仍发现有残存癌细胞的病友,往往面临着更高的复发风险。今天,我们要分享一个足以改写临床指南、为万千家庭带来希望的重磅好消息:ADC领域领军药物Enhertu(T-DXd),在早期乳腺癌领域取得历史性突破!
近日,美国食品药品监督管理局(FDA)宣布,对抗体偶联药物T-DXd(Enhertu)扩展适应症的新申请给予优先审评(Priority Review)资格。该药的新适应症人群为:早期、HER2阳性(意味着适合HER2靶向治疗)乳腺癌患者,术后发现有癌细胞残留,使用T-DXd进行辅助治疗以降低复发风险。3期DESTINY-Breast05临床试验(NCT04622319)结果显示,与目前常用的术后辅助治疗药物T-DM1(Kadcyla)相比,T-DXd可以把患者的疾病复发或死亡风险降低53%,并显著提高3年内不复发的概率。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业















 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估