美国医学前沿
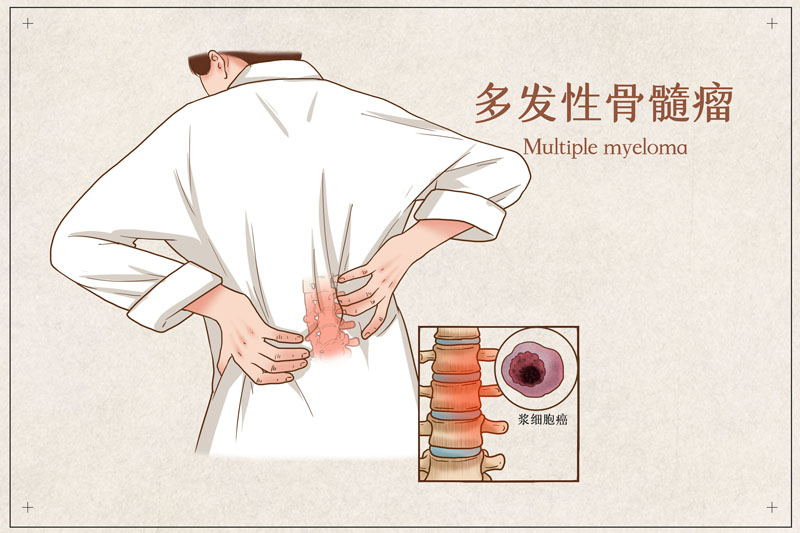
近日,美国纪念斯隆凯特琳癌症中心骨髓瘤项目负责人、国际骨髓瘤基金会科学顾问委员会成员Saad Usmani博士,在接受CURE采访时,介绍了一款名为KTX-1001(又名gintemetostat)的新药,在1期临床试验中,针对一部分多发性骨髓瘤患者的积极进展。
胶质母细胞瘤是一种目前几乎没有有效延长寿命治疗手段的脑部肿瘤,患者的生存时间往往只有短短一年左右。近日,美国弗吉尼亚大学的研究人员发现了一种小分子物质,可以阻断导致胶质母细胞瘤发生和进展的关键基因。这一发现让人们看到了为这种致命的脑癌开发全新治疗方法的希望。
近日,美国食品药品监督管理局(FDA)宣布,授予一种名为Pelareorep的溶瘤病毒疗法快速通道资格(有助于提升研发和审批速度),用于联合贝伐珠单抗和FOLFIRI(标准化疗)方案,二线治疗KRAS突变、微卫星稳定型转移性结直肠癌的患者。
2026年2月2日,美国Exelixis公司宣布,美国食品药品监督管理局(FDA)已接受Zanzalintinib联合Atezolizumab的新药申请,用于治疗既往接受过氟嘧啶类、奥沙利铂和伊立替康方案化疗的成人转移性结直肠癌患者;对于RAS野生型患者,还包括既往接受过抗表皮生长因子受体(EGFR)治疗的人群。FDA给予该申请标准审评,并将处方药使用者付费法案的目标审评日期定为2026年12月3日,意味着FDA将在2026年12月3日前给出是否批准的明确结果。
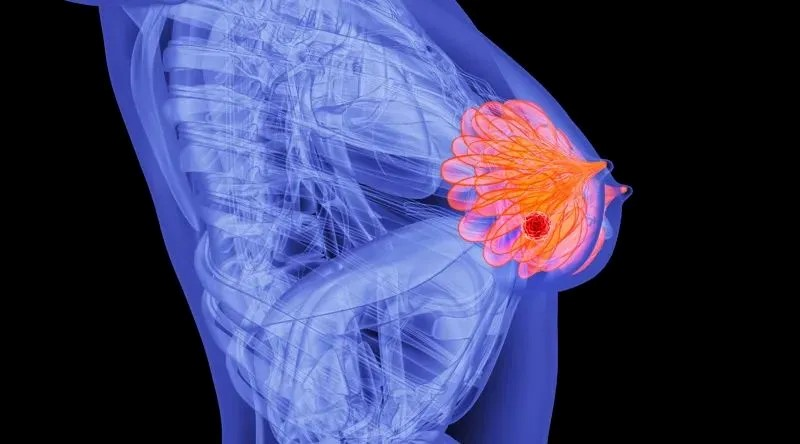
近日,美国妙佑医疗国际(原梅奥诊所)综合癌症中心宣布,其位于美国明尼苏达州和佛罗里达州的院区,已经开始为部分乳腺癌患者及高风险人群,提供一种前沿的机器人辅助保乳头乳腺切除术——该术式已获得美国食品药品监督管理局(FDA)批准。
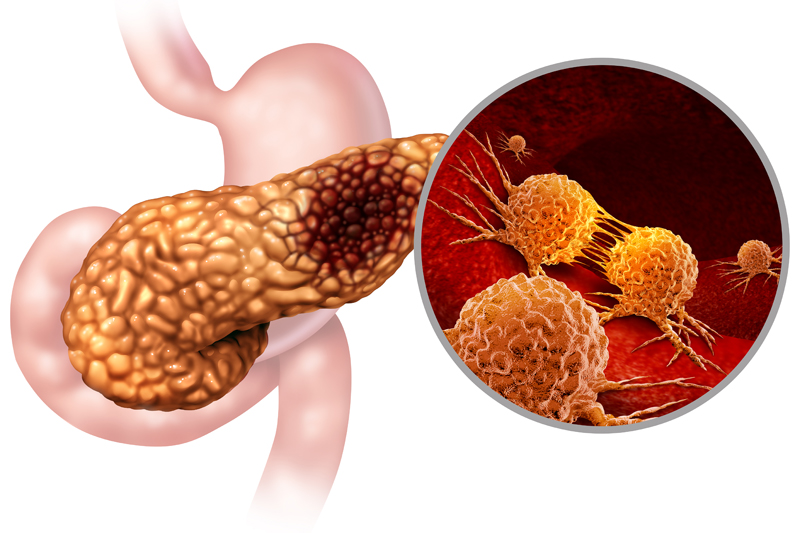
近日,美国Novita Pharmaceuticals公司宣布,美国食品药品监督管理局(FDA)已授予其新药NP-G2-044孤儿药资格,用于治疗胰腺癌。FDA的孤儿药资格授予,旨在支持针对美国少于20万的罕见疾病患者的研究性疗法开发。胰腺癌是致命的恶性肿瘤之一,五年生存率约为12%,尤其在晚期疾病中有效治疗选择十分有限。
近日,美国生物制药公司Quetzal Therapeutics宣布,美国食品药品监督管理局(FDA)已授予QTX-2101快速通道资格,用于治疗急性早幼粒细胞白血病(APL)患者。FDA的快速通道资格,旨在促进严重疾病研究性疗法的开发并加快审评,凸显了急性早幼粒细胞白血病(APL)的严重性及在已有有效标准治疗下仍存在的未满足医疗需求。
很多刚确诊的多发性骨髓瘤患者,会因为年龄或身体状况,不适合做干细胞移植。不能移植,则意味着他们剩下的有效治疗选择十分有限。近日,美国食品药品监督管理局(FDA)新批准上市的一款治疗方案,针对的正是此类患者。研究显示,这款由四种药物组成的四联方案疗效显著,超过一半的患者使用后实现了无癌状态!
RMC-6236(通用名Daraxonrasib),是近几年国内患者高度关注的一款在研抗癌药物,尤其在胰腺癌患者群体中讨论热度极高。该药物可同时覆盖多种KRAS突变类型,在早期临床研究中显示出十分积极的疗效信号。对于长期缺乏有效靶向药选择的患者而言,这是一款被寄予厚望的潜力药物。
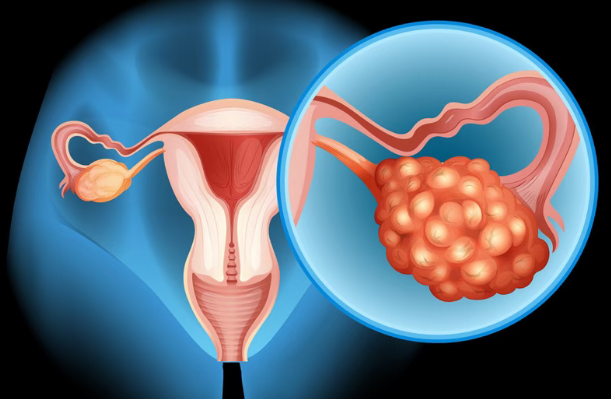
近日,美国Corcept Therapeutics公司宣布,在治疗铂耐药卵巢癌患者的关键性3期ROSELLA试验中,Relacorilant联合白蛋白结合型紫杉醇,达到了总生存期(OS)的主要终点。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业















 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估