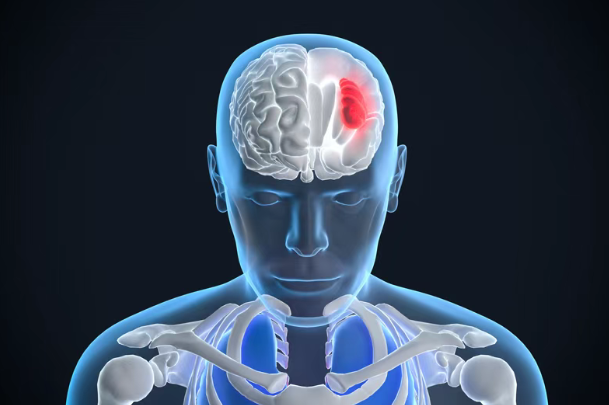
近日,美国Siren Biotechnology公司宣布,美国食品药品监督管理局(FDA)已批准由美国加州大学旧金山分校(UCSF)提交的新药临床试验申请(IND),用于启动一项1期临床研究,评估新药SRN-101在复发性高级别胶质瘤成人患者中的安全性和生物学活性(药物是否在体内发挥作用)。这项1期研究将由加州大学旧金山分校(UCSF)神经外科与神经肿瘤学教授Nicholas Butowski领导。
张雪峰因心源性猝死去世的消息,刺痛了很多人。这样一位仍在工作、仍在运动、看起来还好好的人,为什么会突然倒下?类似的疑问,反复出现在公众讨论中。相比一遍遍的惋惜和震惊,心脏猝死背后的风险、常见误区,以及在关键时刻如何作出更科学的医疗决策,或许才是更值得被看见的内容。去年10月,盛诺一家曾举办【中日心血管诊疗前沿对话】活动,来自中日的两位权威教授,在现场分享了关于心源性猝死的一系列关键认知与前沿观点。
3月24日,峰学蔚来创始人、志愿填报名师张雪峰在公司跑步后出现不适,被紧急送往医院,经抢救无效不幸去世[1]。2026年初,盛诺一家推出了顺天堂医院心脏专项检查服务。通过专项检查项目+权威专家,为广大国人守护生命健康。
近日,欧洲血液与骨髓移植学会(EBMT)第52届年会上公布的2期TRANSCEND FL试验新数据显示,对于已经多次复发、常规治疗逐渐失效的滤泡性淋巴瘤患者,前沿CAR-T疗法(名为liso-cel)疗效显著,97%的患者肿瘤大幅缩小或消失,其中94%的人肿瘤全消失。
小细胞肺癌、小细胞前列腺癌,以及部分具有神经内分泌特征的卵巢癌,都属于侵袭性很强的同一类肿瘤。它们往往发展快、容易转移且治疗难度大。近日,美国加州大学洛杉矶分校(UCLA)在《美国国家科学院院刊》发表的研究显示:小细胞神经内分泌癌常因缺失关键抑癌基因RB而变得更加凶险,但与此同时,也暴露出一个新的致命弱点。
骨髓移植是血液肿瘤患者的治疗方法之一。但一部分患者在移植后,却出现了一个棘手的问题,叫移植物抗宿主病。简单说,就是移植进来的新免疫系统不认人,反过来攻击患者自己的身体。如果这种攻击发生在肠道,就叫胃肠道型急性移植物抗宿主病。患者会出现严重腹泻、腹痛,甚至肠道出血,情况可能非常凶险。常规治疗通常先用糖皮质激素去压制这种过度免疫反应,如果无效,再用一种叫ruxolitinib的靶向药。但问题是,一旦这两步都失败,后面几乎没有被正式批准的治疗手段。陷入这个阶段的患者中,一半人的生存时间不到86天。
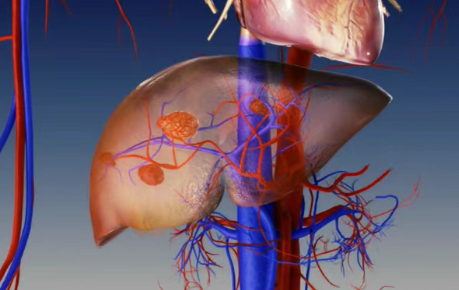
肝细胞癌(HCC)一直是临床治疗中的难点之一。多数患者在确诊时已失去手术机会,只能依赖局部或全身治疗来控制病情。长期以来,经肝动脉化疗栓塞(TACE)被视为这一阶段的主要治疗手段,但疗效始终存在瓶颈。2025年7月,SIR-Spheres Y-90树脂微球(中文称作钇-90)获得美国食品药品监督管理局(FDA)批准,用于治疗不可切除的肝细胞癌(HCC)。
3月20日,据百时美施贵宝新闻稿报道,美国食品药品监督管理局(FDA)批准纳武利尤单抗(nivolumab,商品名Opdivo)联合AVD化疗,用于成人及12岁以上、既往未治疗的Ⅲ/Ⅳ期经典型霍奇金淋巴瘤患者。对刚被确诊、正站在人生岔路口的患者和家属来说,这条消息的分量很直接:未来,晚期经典型霍奇金淋巴瘤的一线治疗,出现了一个更强、更有希望的新标准。
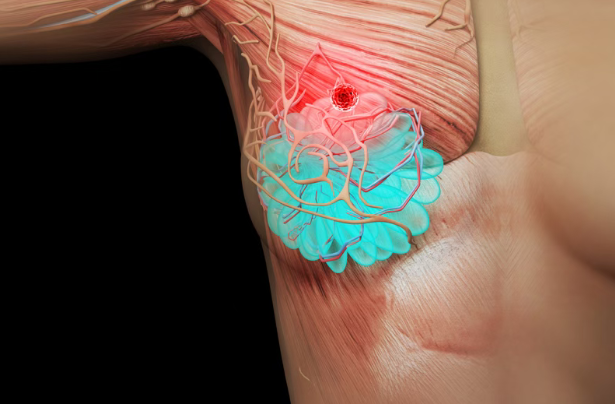
近日,美国Celcuity公司公布了其开发的新药Gedatolisib,在3期VIKTORIA-1临床试验中PIK3CA野生型患者队列的疗效和安全性结果。该队列包括激素受体阳性(HR+)、人表皮生长因子受体2阴性(HER2-)、PIK3CA野生型的晚期乳腺癌患者,这些患者在接受CDK4/6抑制剂和芳香化酶抑制剂治疗期间或之后出现疾病进展。研究结果显示,在PIK3CA野生型晚期乳腺癌中,Gedatolisib联合Fulvestrant(以及联合Palbociclib),可显著改善无进展生存期,意味着有效帮助患者控制了疾病进展。研究结果发表于医学学术期刊《临床肿瘤学杂志》上。
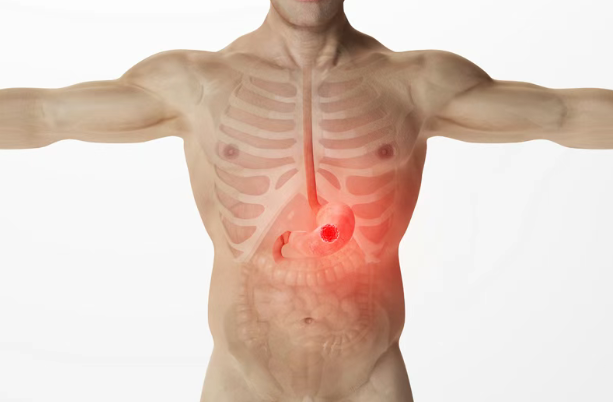
近日,美国NovaBridge Biosciences公司宣布,已就新药Givastomig在一线HER2阴性、CLDN18.2阳性、PD-L1阳性胃癌/胃食管交界癌患者中的加速批准潜力,与美国食品药品监督管理局(FDA)达成一致意见。这一进展基于近期公布的1b期临床试验(临床试验注册号:NCT04900818)剂量扩展数据基础上。这是Givastomig首次用于人体研究,主要评估其在晚期实体瘤中的安全性、耐受性、药代动力学、药效学以及初步抗肿瘤活性,包括单药和联合治疗方案。研究结果显示,Givastomig疗效显著且耐受性良好。
 红杉资本(中国)被投企业
红杉资本(中国)被投企业








 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估