小细胞肺癌真的有药了!6款新药强势突围,有效率突破90%
发布时间:2025-08-05 作者:盛诺一家 更新时间:2025-08-05
本文由盛诺一家原创编译,转载需经授权
摘要
小细胞肺癌(SCLC)是一种高度侵袭性、进展迅速的肺癌类型,但近年来其治疗策略正在发生深刻变化。
本文综述了小细胞肺癌治疗领域的三项重要进展,包括:
局限期小细胞肺癌(SCLC)中,免疫巩固治疗带来了新的治疗选择;
广泛期小细胞肺癌(ES-SCLC)方面,化疗联合免疫治疗已确立为一线标准方案;
在复发或耐药阶段,靶向药物和T细胞连接器等新型免疫疗法迅速崛起,相关临床试验显示出令人鼓舞的疗效。
这些新疗法不仅提高了治疗效果,也预示着未来小细胞肺癌治疗将朝着更加个体化、精准化的方向发展。随着治疗手段的不断丰富与升级,小细胞肺癌患者的生存前景正在一步步改善。
来源:ChatGPT生成AI示意图
1.免疫巩固治疗正在重新定义局限期小细胞肺癌(LS-SCLC)的治疗标准
局限期小细胞肺癌(LS-SCLC)是指癌细胞仅局限在一侧胸腔及其附近区域,仍可通过单一放疗照射范围覆盖的早期阶段。
巩固治疗是指在主要治疗(如化疗或放疗)成功控制肿瘤后,为进一步清除体内残余癌细胞、降低复发风险而追加的一种强化治疗。它不是起始治疗,而是“稳固成果、防止反弹”的后续步骤。
来自3期ADRIATIC试验的结果,为I至III期且同步化放疗后未进展的LS-SCLC患者提供了新的治疗选择。
患者被随机分配接受Durvalumab、Durvalumab+Tremelimumab或安慰剂巩固治疗。
Durvalumab是一种抗PD-L1免疫检查点抑制剂,Tremelimumab是一种CTLA-4免疫检查点抑制剂,两者联合用于增强免疫系统对抗癌细胞的能力。
✅研究结果
Durvalumab组的平均总生存期(OS)为55.9个月,安慰剂组为33.4个月。风险比HR为0.73,意味着Durvalumab组的死亡风险比安慰剂组低了27%。
Durvalumab组的平均无进展生存期(PFS)为16.6个月,意味着一半患者在16.6个月内病情没有恶化;安慰剂组为9.2个月。风险比HR为0.76,意味着Durvalumab组的疾病进展或死亡风险比安慰剂组低了24%。
✅安全性
Durvalumab组3级或4级严重不良反应的发生率为24.4%,安慰剂组为24.2%。
Durvalumab组与治疗相关的死亡发生率为0.8%,安慰剂组为0%。
Durvalumab组免疫介导的3级或4级不良反应(指免疫治疗激活免疫系统后引发的严重或危及生命的副作用)的发生率为53%,安慰剂组为1.5%。
ADRIATIC试验中蕞常见的不良反应为放射性肺炎:Durvalumab组的发生率为38.2%,安慰剂组为30.2%。大多数为轻微的1级或2级。
来源:ChatGPT生成AI示意图
2.广泛期小细胞肺癌(ES-SCLC)的一线治疗标准已变为化疗+免疫治疗,但仍有挑战
广泛期小细胞肺癌(ES-SCLC)是指癌细胞已扩散到胸腔两侧或身体其他部位,无法通过单一放疗照射范围控制的晚期疾病。
对于ES-SCLC患者,化疗联合免疫治疗已成为标准治疗方案,多个3期试验支持这一结论。
3期CASPIAN研究显示,PD-L1免疫检查点抑制剂Durvalumab联合化疗相比单独化疗,可改善总生存期(OS)。
3期IMpower133研究显示,PD-L1免疫检查点抑制剂Atezolizumab联合化疗,相比安慰剂+化疗,也带来生存获益。
3b期MAURIS研究评估了Atezolizumab+Carboplatin/Etoposide化疗方案,在154例ES-SCLC患者中的实际应用情况。
✅研究结果
平均总生存期(OS)为10.7个月。
平均无进展生存期(PFS)为5.5个月,意味着一半患者在5.5个月内病情没有恶化。
客观缓解率(ORR)为71.6%,意味着有71.6%的患者肿瘤显著缩小或完全消失。
✅安全性
29.9%的患者发生了严重不良反应。
14.9%的患者出现了免疫相关不良反应。
目前还有一些治疗上的问题正在研究中,比如是否需要给大脑做预防放疗、怎么安排后续维持治疗,以及是否可以根据患者自身特征来制定更精准的一线治疗方案。
3.一线化疗后,靶向药和T细胞连接器正成为新选择
对于在一线化疗后复发或耐药的小细胞肺癌患者,治疗手段日益丰富。
①Lurbinectedin(芦比替定)
Lurbinectedin
(来源:博鳌乐城医疗先行区中心药房公众号)
Lurbinectedin依旧是美国NCCN指南推荐的重要二线治疗。
1/2期LUPER研究评估了Lurbinectedin+Pembrolizumab(PD-1抑制剂)联合方案的疗效。
✅研究结果
12名患者中:
1名患者达到完全缓解(CR),即肿瘤完全消失。
3名患者达到部分缓解(PR),即肿瘤显著缩小。
3名患者疾病获得稳定。
疾病控制率(DCR)为61.5%。
✅安全性
2人因免疫相关不良反应停用Pembrolizumab。
剂量限制毒性包括1例3级乏力和1例4级中性粒细胞减少(持续3天以上)。
②Tarlatamab(塔拉妥单抗)
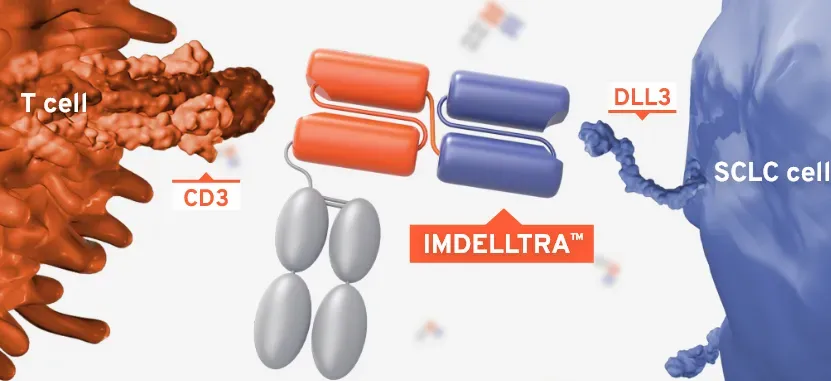
Tarlatamab(塔拉妥单抗)是一种DLL3xCD3 T细胞连接器,因其在DeLLphi-301 2期研究中展现出持久疗效,已被批准用于接受过铂类治疗的小细胞肺癌患者。
✅研究结果
在10 mg剂量组中,客观缓解率(ORR)为40.4%,意味着有40.4%的患者肿瘤显著缩小或完全消失。
平均缓解持续时间(DOR)为9.7个月,意味着对治疗有反应的患者,肿瘤平均能被控制大约9.7个月。
平均无进展生存期(PFS)为4.3个月,意味着一半患者在4.3个月内病情没有恶化。
平均总生存期(OS)为15.2个月。
✅安全性
Tarlatamab的不良反应中,细胞因子释放综合征(CRS)和免疫效应细胞相关神经毒性综合征(ICANS)需特别关注。
在DeLLphi-301试验中,CRS通常出现在第1个疗程的第1或第2次用药后。整体上,32%的患者出现1级CRS(轻度),20%为2级(中度),1%为3级(重度)。
ICANS通常在前6个月内发生。10%的患者出现1级ICANS(轻度),5%为2级(中度)。
③Obrixtamig(BI 764532)
Obrixtamig(BI 764532)是另一种DLL3xCD3双特异T细胞连接器,在一项1期研究中,展现出积极疗效。该研究共纳入24名小细胞肺癌患者。
✅研究结果
客观缓解率(ORR)为33%,意味着有33%的患者肿瘤显著缩小或完全消失。
✅安全性
共报告6例剂量限制性毒性,包括3级意识混乱(重度)、3/4级细胞因子释放综合征(CRS)(重度/危及生命)、3级神经系统障碍(重度)和2级输注反应(中度)。
1-2级CRS(轻中度)的发生率为58%,可通过支持治疗、激素或IL-6R抗体药物控制。
来源:ChatGPT生成AI示意图
④HPN328
HPN328是一种三特异T细胞激活构建体(TriTAC),靶向DLL3、CD3和白蛋白,在一项1/2a期试验中展现出积极效果。
✅研究结果
在9名DLL3阳性小细胞肺癌患者中,3名患者获得部分缓解(PR),即肿瘤显著缩小(超过30%)。
✅安全性
31%的患者在初次或第二次用药后24小时内出现1级或2级细胞因子释放综合征(CRS)(轻中度)。
此外,还有其他多款在研疗法。例如:
⑤Ifinatamab deruxtecan(I-DXd)
Ifinatamab deruxtecan(I-DXd)是一种抗体偶联药物(ADC)。
在2期IDeate-Lung01研究中,42名广泛期小细胞肺癌(ES-SCLC)患者接受12 mg/kg剂量后:
客观缓解率(ORR)为54.8%,意味着有54.8%的患者肿瘤显著缩小或完全消失。
疾病控制率为90.5%。
⑥ABBV-706
ABBV-706是一种靶向SEZ6的抗体偶联药物(ADC)。
在一项1期研究中,在22名小细胞肺癌患者中:
客观缓解率(ORR)为40%,意味着有40%的患者肿瘤显著缩小或完全消失。
安全性方面,2名患者出现剂量限制性毒性,其中1例为4级白细胞和中性粒细胞减少(危及生命,超过7天),1例为4级血小板减少(危及生命)。

来源:ChatGPT生成AI示意图
复发后的治疗选择应综合考虑既往用药、合并症和功能状态。新型靶向药和T细胞连接器的加入,有望重塑小细胞肺癌治疗顺序与个体化治疗路径。
来源:
https://www.cancernetwork.com/view/3-things-you-should-know-about-evolving-strategies-in-sclc-limited-stage-advances-frontline-innovation-and-postplatinum-progress
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者首选盛诺一家?
- 官方资质:与美国、日本、英国近50家TOP级医院签署官方合作协议,搭建全球医疗服务网络
- 全球就医:跳出单一国家视野、整合全球专家智慧、规划匹配最优就医路径,追求更佳医疗结果
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-875-6700,或通过 盛诺一家官网 预约咨询!
本文为海外就医科普文章,内容仅供阅读参考,不作为任何疾病治疗的指导意见。文章由盛诺一家编译,版权归盛诺一家公司所有,转载或引用本网内容须注明"转自盛诺一家官网(www.stluciabj.cn)"字样。
- 相关资讯
- 最新动态
 红杉资本(中国)被投企业
红杉资本(中国)被投企业













 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估