美国前沿药Amezalpat获快速通道资格,治疗肝癌效果突出,势头强劲!
发布时间:2025-02-14 作者:盛诺一家 更新时间:2025-02-14
摘要
美国食品药品监督管理局(FDA)授予前沿药Amezalpat快速通道资格,作为肝细胞癌(HCC)患者的潜在治疗选择。
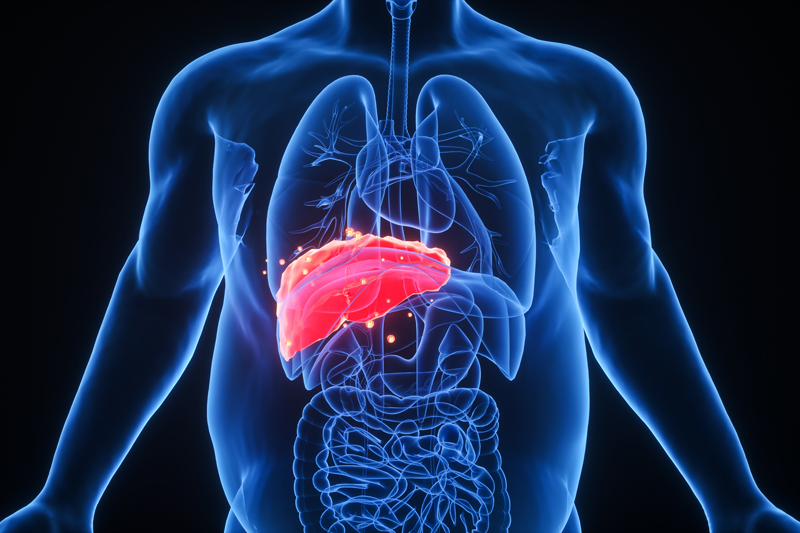
关于肝细胞癌(HCC)
肝细胞癌(HCC)是一种侵袭性癌症,死亡率不断上升,预计到2030年将成为全球癌症死亡的第三大原因。全球每年有超过90万人被诊断为HCC。HCC的发病率和死亡率在东亚地区蕞高,并在欧洲和美国的某些地区呈上升趋势。
临床试验情况
阿替利珠单抗(atezolizumab)是一种PD-L1免疫检查点抑制剂,贝伐单抗(bevacizumab)是一种抗VEGF单抗药物。
已公布数据结果
美国FDA的孤儿药资格是指针对罕见疾病的治疗药物,获得FDA的特别认证,旨在促进这些药物的研发和审批,以便为患者提供治疗选择。
专家评论
来源:
https://www.onclive.com/view/fda-grants-fast-track-designation-to-amezalpat-for-hepatocellular-carcinoma
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者首选盛诺一家?
- 官方资质:与美国、日本、英国近50家TOP级医院签署官方合作协议,搭建全球医疗服务网络
- 全球就医:跳出单一国家视野、整合全球专家智慧、规划匹配最优就医路径,追求更佳医疗结果
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-875-6700,或通过 盛诺一家官网 预约咨询!
本文为海外就医科普文章,内容仅供阅读参考,不作为任何疾病治疗的指导意见。文章由盛诺一家编译,版权归盛诺一家公司所有,转载或引用本网内容须注明"转自盛诺一家官网(www.stluciabj.cn)"字样。
- 相关资讯
- 最新动态
 红杉资本(中国)被投企业
红杉资本(中国)被投企业













 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估