重磅!头款难治性卵巢癌ADC药物获FDA加速批准
发布时间:2022-11-16 作者:盛诺一家 更新时间:2023-07-12
导读
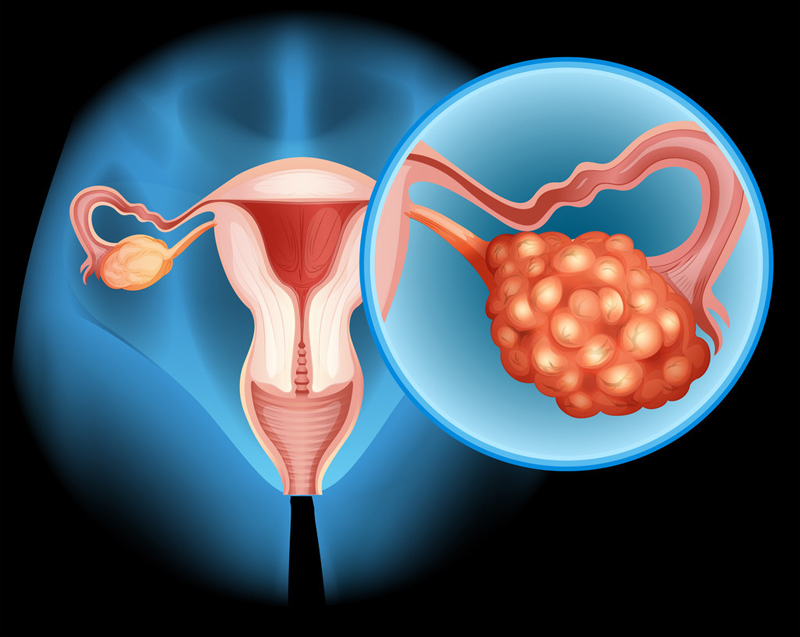
头款难治性卵巢癌抗体偶联药物(ADC)Elahere获FDA加速批准,使得31.7%的患者肿瘤大幅度缩小,4.8%的患者肿瘤完全消失。
近日,美国FDA加速批准了Elahere(mirvetuximab soravtansine-gynx)治疗FRα阳性、铂类耐药的上皮性卵巢癌、输卵管癌或原发性腹膜癌成人患者,要求这些患者既往接受过1~3线全身治疗。

Ursula Matulonis医生
【盛诺一家】成立于2011年,是国内领先的海外医疗咨询服务机构,至今已为近10000个患者家庭提供出国就医服务,重点涵盖癌症、心脏病、罕见疾病等重疾领域。凭借专业、贴心、高效的服务,盛诺一家赢得了99%客户好评率!
📌为什么出国就医患者首选盛诺一家?
- 官方资质:与美国、日本、英国近50家TOP级医院签署官方合作协议,搭建全球医疗服务网络
- 全球就医:跳出单一国家视野、整合全球专家智慧、规划匹配最优就医路径,追求更佳医疗结果
- 专业可靠:咨询服务团队成员70%拥有医学背景,包括医学院博士、三甲医院医生、资深医学翻译
- 一站式服务:在全球设有15个客户服务中心,保障从国内到海外全流程、高品质的服务质量
- 客户至上:推出48小时冷静期、风险告知书、医疗费用“零加成”等措施,保障客户权益
- 专属折扣:通过本公司预约出国就医的患者,可额外申请5%–40%的医疗费用减免折扣
👉如果您或者家人需要出国看病,可拨打免费咨询热线 400-875-6700,或通过 盛诺一家官网 预约咨询!
本文为海外就医科普文章,内容仅供阅读参考,不作为任何疾病治疗的指导意见。文章由盛诺一家编译,版权归盛诺一家公司所有,转载或引用本网内容须注明"转自盛诺一家官网(www.stluciabj.cn)"字样。
- 相关资讯
- 最新动态
 红杉资本(中国)被投企业
红杉资本(中国)被投企业













 咨询医学顾问——免费获取全球医疗评估方案!
咨询医学顾问——免费获取全球医疗评估方案!
 提交成功!
提交成功!


 出国看病费用评估
出国看病费用评估